อนาคตของเลือดเทียม
จากความฝันในห้องแล็บสู่ความเป็นจริงในโรงพยาบาล
จุดเริ่มต้นของการแสวงหา
การวิจัยเลือดทดแทนไม่ใช่เรื่องใหม่ แต่มันคือภารกิจทางวิทยาศาสตร์ที่ดำเนินมากว่าหลายสิบปี เหตุผลนั้นเรียบง่ายแต่สำคัญ—ระบบบริจาคเลือดในปัจจุบันมีข้อจำกัดชัดเจน ทั้งเรื่อง อายุการเก็บรักษาที่สั้น ความเสี่ยงจากการถ่ายเลือด และปัญหาการขาดแคลนในสถานการณ์ฉุกเฉิน
ในสถานการณ์อย่างสงคราม ภัยพิบัติ หรืออุบัติเหตุร้ายแรง ความต้องการเลือดมักสูงกว่าปริมาณที่มีอยู่ นั่นทำให้เป้าหมายสูงสุด หรือ “Holy Grail” ของนักวิจัย คือการสร้างเลือดที่ ใช้ได้กับทุกหมู่เลือด เก็บได้นานที่อุณหภูมิห้อง ปลอดเชื้อ และพร้อมใช้งานทันที
แต่เส้นทางนี้ไม่ได้ราบรื่น ความล้มเหลวของโครงการรุ่นแรกและความท้าทายด้านความปลอดภัยทำให้วงการต้องปรับกลยุทธ์ จากการสร้าง “สารทดแทนเลือดเต็มรูปแบบ” ไปสู่การพัฒนา สารพาหะออกซิเจน (Oxygen Therapeutics) ที่เน้นแก้ปัญหาเฉพาะจุดและใช้ในสถานการณ์เฉพาะ
1. ฮีโมโกลบินไร้เซลล์ (HBOCs) – จากบทเรียนราคาแพงสู่โอกาสใหม่
HBOCs ทำงานโดยนำโปรตีนฮีโมโกลบินออกมาทำหน้าที่นอกเซลล์เม็ดเลือดแดง ซึ่งมีข้อดีหลายอย่าง เช่น เก็บได้นานกว่าปี ใช้ได้ทุกหมู่เลือด และสามารถฆ่าเชื้อได้เต็มรูปแบบ
อย่างไรก็ตาม รุ่นแรกของ HBOCs ต้องเผชิญกับปัญหาหนัก เช่น
- ภาวะหลอดเลือดหดตัว จากการจับไนตริกออกไซด์
- พิษต่อไต จากโมเลกุลขนาดเล็กที่กรองผ่านไต
- ภาวะเครียดออกซิเดชัน ที่ทำลายเนื้อเยื่อ
ผลลัพธ์คือการยุติการทดลองหลายโครงการ รวมถึง Polyheme® ที่พบอัตราการเสียชีวิตสูงกว่าที่คาด
การพัฒนารุ่นใหม่
เพื่อลดความเสี่ยงเหล่านี้ นักวิจัยได้พัฒนากลยุทธ์ใหม่ เช่น
- Polymerization – เพิ่มขนาดโมเลกุล ลดการรั่วออกนอกหลอดเลือด เช่น Hemopure®
- PEGylation – เคลือบโมเลกุลเพื่อลดผลข้างเคียง เช่น Hemospan®
- Encapsulation – ห่อหุ้มฮีโมโกลบินในไลโปโซมให้เลียนแบบเซลล์เม็ดเลือดแดง
นวัตกรรมที่โดดเด่นคือ M101 จากฮีโมโกลบินของหนอนทะเล Arenicola marina ซึ่งมีโมเลกุลใหญ่กว่ามนุษย์ถึง 250 เท่า ปลอดภัยต่อไต และไม่ทำให้หลอดเลือดหดตัว จุดเด่นคือนำไปใช้สำเร็จใน การถนอมอวัยวะก่อนปลูกถ่าย ช่วยให้การใช้งานปลอดภัยมากขึ้น
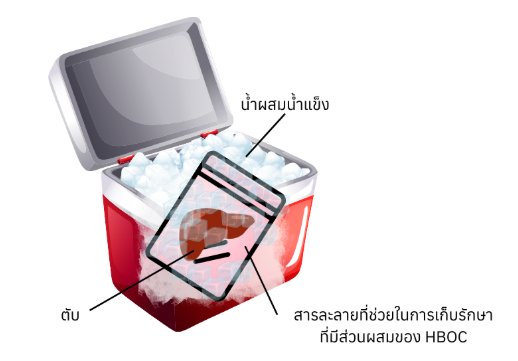
การเก็บรักษาตับที่ถูกแยกออกมาในสภาวะเย็นแบบนิ่ง (Static Cold Preservation) หลังจากทำการเติมออกซิเจนล่วงหน้าด้วยสารละลายถนอมอวัยวะที่ผสม ฮีโมโกลบินไร้เซลล์ (HBOC) เพื่อเพิ่มปริมาณออกซิเจนในเนื้อเยื่อก่อนการปลูกถ่าย
2. เพอร์ฟลูออโรคาร์บอน (PFCs) – สารสังเคราะห์เฉื่อยที่ละลายก๊าซได้
ต่างจากฮีโมโกลบิน PFCs ไม่จับออกซิเจน แต่ละลายก๊าซได้ในปริมาณมาก จึงต้องใช้งานในสภาวะที่มีออกซิเจนสูง และอยู่ในรูปอิมัลชันเพื่อให้เข้ากับร่างกาย แม้ผลิตภัณฑ์รุ่นแรกอย่าง Fluosol-DA จะล้มเหลวเพราะผลข้างเคียงและปัญหาการเก็บรักษา แต่ Perftoran® ยังคงได้รับการใช้งานในบางประเทศ เช่น รัสเซียและเม็กซิโก สะท้อนถึงความแตกต่างด้านกฎระเบียบระหว่างภูมิภาค
3. การสร้างเม็ดเลือดแดงในห้องปฏิบัติการ – ก้าวใหม่จากโครงการ RESTORE
ในสหราชอาณาจักร โครงการ RESTORE ได้ทดลองเพาะเลี้ยงเม็ดเลือดแดงจากเซลล์ต้นกำเนิดของผู้บริจาค กระบวนการนี้ใช้เวลาประมาณ 3 สัปดาห์ก่อนจะได้เซลล์เม็ดเลือดแดง “สดใหม่ทั้งหมด” คำถามสำคัญคือ เซลล์เหล่านี้จะมีอายุในร่างกายนานกว่าเลือดทั่วไปหรือไม่ หากได้ผลจริง อาจลดความถี่การถ่ายเลือดสำหรับผู้ป่วยโรคเรื้อรัง เช่น ธาลัสซีเมีย หรือซิกเคิลเซลล์
4. เลือดเฉพาะบุคคลจาก iPSC – ความก้าวหน้าที่ MCRI ออสเตรเลีย
ปี 2024 ถือเป็นจุดเปลี่ยนเมื่อทีมวิจัย MCRI สามารถสร้าง เซลล์ต้นกำเนิดเม็ดเลือด (HSC) จากเซลล์ของผู้ป่วยเอง ผ่านเทคโนโลยี induced Pluripotent Stem Cells (iPSC) และปลูกถ่ายติดในไขกระดูกสัตว์ทดลองได้สำเร็จ นี่ไม่ใช่เพียงการผลิตเลือดในถุง แต่คือการสร้าง “โรงงานผลิตเลือด” ภายในร่างกาย ที่สามารถสร้างเม็ดเลือดได้ตลอดชีวิตของผู้ป่วย ซึ่งมีศักยภาพรักษาโรคเลือดพันธุกรรมให้หายขาดได้
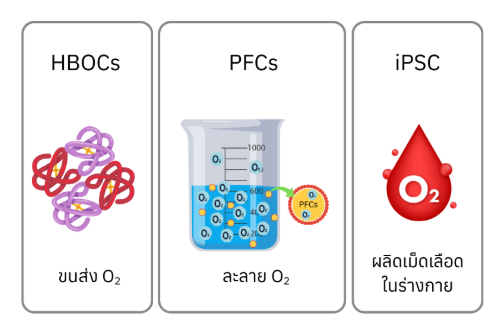
การทำงานของเทคโนโลยีหลักในการทดแทนหรือเสริมการทำงานของเลือด ได้แก่ HBOCs ใช้ฮีโมโกลบินนอกเซลล์ในการขนส่งออกซิเจน, PFCs เป็นสารสังเคราะห์ที่ละลายออกซิเจนได้ในปริมาณสูง และ iPSC ใช้เทคโนโลยีเซลล์ต้นกำเนิดเพื่อผลิตเซลล์เม็ดเลือดในร่างกายอย่างต่อเนื่อง
ความท้าทายและเส้นทางข้างหน้า
แม้เทคโนโลยีเลือดเทียมจะก้าวหน้าอย่างน่าทึ่งในช่วงไม่กี่ปีที่ผ่านมา แต่เส้นทางสู่การใช้งานอย่างแพร่หลายยังเต็มไปด้วยอุปสรรค ทั้งในเชิงเศรษฐกิจ กฎระเบียบ และการยอมรับจากวงการแพทย์
หนึ่งในความท้าทายใหญ่ที่สุดคือ ต้นทุนการผลิต — เลือดที่เพาะเลี้ยงในห้องปฏิบัติการอาจมีราคาสูงถึง 15,000 ดอลลาร์สหรัฐต่อยูนิต เมื่อเทียบกับเลือดบริจาคที่มีราคาถูกกว่าหลายสิบเท่า สำหรับการผ่าตัดทั่วไป ตัวเลขนี้อาจดูเกินเอื้อม แต่ในมุมของผู้ป่วยโรคเลือดเรื้อรังที่ต้องถ่ายเลือดทุก 3–4 สัปดาห์ไปตลอดชีวิต ต้นทุนรวมจากการรักษาในระยะยาวอาจสูงยิ่งกว่า การปลูกถ่าย HSC จาก iPSC เพียงครั้งเดียวที่อาจรักษาให้หายขาด จึงอาจกลายเป็นทางเลือกที่คุ้มค่าในภาพรวม
นอกจากเรื่องต้นทุนแล้ว กฎระเบียบด้านความปลอดภัย ก็เป็นอีกด่านสำคัญ ประเทศต่าง ๆ มีมาตรฐานและกระบวนการอนุมัติที่แตกต่างกัน บางประเทศพร้อมเปิดทางให้เทคโนโลยีที่มีความเสี่ยงต่ำกว่า เช่น การใช้ HBOCs ในการถนอมอวัยวะหรือในสถานการณ์ฉุกเฉิน ขณะที่อีกหลายประเทศยังตั้งเกณฑ์ความปลอดภัยสูงจนยากจะผ่านการอนุมัติ
ในอีกด้านหนึ่ง เทคโนโลยีเสริมกำลังเข้ามาช่วยเร่งให้การจัดการเลือดมีประสิทธิภาพมากขึ้น เช่น AI และ Machine Learning ที่สามารถคาดการณ์ความต้องการเลือดในระดับโรงพยาบาลหรือภูมิภาค ลดการสูญเสียและเพิ่มความแม่นยำในการจัดสรร รวมถึงการวิเคราะห์ภาพฟิล์มเลือดโดยอัตโนมัติเพื่อช่วยวินิจฉัยโรคเลือดต่าง ๆ ซึ่งเป็นการใช้ทรัพยากรที่มีอยู่ให้เกิดประโยชน์สูงสุด ควบคู่ไปกับการพัฒนาเทคโนโลยีใหม่ ๆ
04เมื่อมองไปข้างหน้า อนาคตของความมั่นคงด้านเลือดคงไม่อาศัย “ผู้ชนะเพียงหนึ่งเดียว” แต่จะเป็นการผสมผสานของหลายเทคโนโลยีเข้าด้วยกัน — ตั้งแต่เลือดบริจาคที่จัดการด้วยระบบอัจฉริยะ, สารพาหะออกซิเจนสำหรับเหตุการณ์เฉพาะทาง, เลือดเพาะเลี้ยงสำหรับผู้ป่วยกลุ่มยากต่อการถ่ายเลือด, ไปจนถึงการรักษาโรคเลือดพันธุกรรมที่ต้นเหตุด้วย iPSC
นี่คือภาพของอนาคตที่การเข้าถึงเลือดจะมีความ ยืดหยุ่น ปลอดภัย และตอบสนองได้ต่อทุกสถานการณ์ ไม่ว่าจะเป็นในห้องฉุกเฉิน โรงผ่าตัด หรือพื้นที่ภัยพิบัติ — และนั่นคือเป้าหมายที่วงการแพทย์ทั่วโลกกำลังเดินหน้าไปสู่

ในอนาคต หากทีมกู้ภัยสามารถเข้าถึงเลือดและเทคโนโลยีเลือดเทียมที่พร้อมใช้ในทุกสถานการณ์ ผู้บาดเจ็บในพื้นที่ภัยพิบัติจะมีโอกาสรอดชีวิตสูงขึ้น ได้รับการส่งออกซิเจนและการรักษาอย่างต่อเนื่องตั้งแต่จุดเกิดเหตุจนถึงโรงพยาบาล
Work cited
- Blood Substitutes - ResearchGate, accessed August 6, 2025
- Artificial Oxygen Carriers—Past, Present, and Future—a Review of the Most Innovative and Clinically Relevant Concepts, accessed August 6, 2025
- Blood substitutes- the polyheme trials - PMC, accessed August 6, 2025
- Progress in Development of Functional Biological and Synthetic Blood Products to Augment Transfusable Blood Supply in Operational Medicine, accessed August 6, 2025
- Blood Substitutes: How Close to a Solution? - CancerNetwork, accessed August 6, 2025
- Tracking Research on Hemoglobin-Based Oxygen Carriers: A Scientometric Analysis and In-Depth Review, accessed August 6, 2025
- LETTER TO EDITOR MARINE RESOURCES: POTENTIAL OF POLYCHAETE APPLICATION IN COMBATING COVID-19 INFECTION - JSSM, accessed August 6, 2025
- Complement-Mediated Acute Effects of Liposome-Encapsulated Hemoglobin, accessed August 6, 2025
- marine resources: potential of polychaete application in combating covid-19 infection, accessed August 6, 2025
- World-First Trial Transfusing Lab-Grown Red Blood Cells Begins, accessed August 6, 2025
- Blood stem cell breakthrough could transform bone marrow transplants - Murdoch Children's Research Institute, accessed August 6, 2025
- Lab-developed blood stem cell success in Australia - British Society for Haematology, accessed August 6, 2025
- reNEW researchers lead world-first blood stem cell breakthrough, accessed August 6, 2025
- Blood stem cell breakthrough could transform bone marrow transplants - University of Birmingham, accessed August 6, 2025
- Lab-grown blood stem cells - News - Nature Middle East, accessed August 6, 2025
- Development of blood demand prediction model using artificial intelligence based on national public big data, accessed August 6, 2025
- From microscope to micropixels: A rapid review of artificial intelligence for the peripheral blood film - PubMed, accessed August 6, 2025
- Artificial intelligence for the detection of acute myeloid leukemia from microscopic blood images; a systematic review and meta-analysis - PubMed, accessed August 6, 2025
- Machine learning in transfusion medicine: A scoping review - PMC, accessed August 6, 2025
